灣區時訊 1 月 16 日,NMPA 官網公示,奧賽康遞交的利厄替尼(ASK120067 片)上市申請已獲得批準(CXHS2101052),適用于既往經表皮生長因子受體(EGFR)酪氨酸激酶抑制劑(TKI)治療時或治療后出現疾病進展,并且經檢測確認存在 EGFR T790M 突變陽性的局部晚期或轉移性非小細胞肺癌(NSCLC)成人患者的治療。
截圖來源:NMPA官網
肺癌是中國發病率、死亡率最高的惡性腫瘤,表皮生長因子受體(EGFR)是 NSCLC 中最常見的驅動基因,30%~50% 的亞裔 NSCLC 患者存在 EGFR 基因突變。第三代 EGFR 抑制劑是治療 EGFR 基因突變 NSCLC 的有效選擇之一。
利厄替尼是一款第三代表皮生長因子受體酪氨酸激酶抑制劑 (EGFR-TKI),由中國科學院上海藥物研究所、中國科學院廣州生物醫藥與健康研究院、奧賽康藥業聯合開發,擬開發用于治療 EGFR 突變NSCLC。信達生物擁有中國大陸地區獨家推廣銷售權。
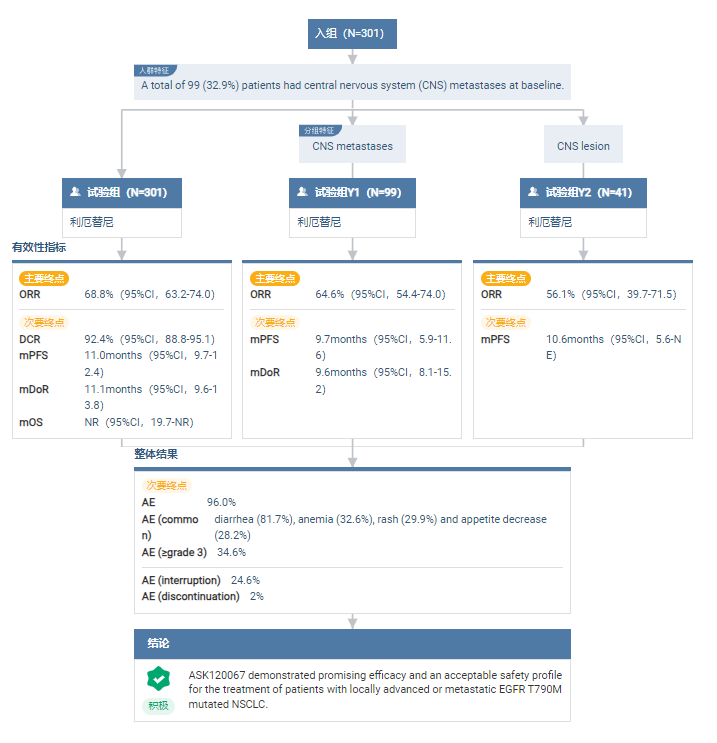
在 2022 年 ASCO 年會上,奧賽康曾公布了利厄替尼在既往 EGFR-TKI 治療后進展的 T790M+局部晚期或轉移性 NSCLC 患者中的單臂 IIb 期臨床研究數據(NCT03502850)。該研究共納入了來自 62 家中心的 301 例患者。其中,61.1% 和 33.2% 的患者分別為 EGFR 19del 突變和 EGFR L858R 突變,32.9% 的患者為無癥狀、穩定的腦轉移(CNS)患者。
研究結果顯示:
經獨立評審委員會(IRC)評估的客觀緩解率(ORR)為 68.8%,疾病控制率(DCR)為 92.4%,緩解持續時間(DoR)為 11.1 個月,無進展生存期(PFS)為 11.0 個月。總生存期(OS)數據尚未成熟。
CNS 患者顱內 ORR 為 56.1%,CNS 患者 PFS 為 10.6 個月,這意表明 ASK120067 片對 CNS 患者具有較好的療效。
患者安全耐受性良好,絕大部分患者會發生不良反應,但多為 1 級或 2 級。
利厄替尼IIb 期研究總覽圖
截圖來自:Insight 數據庫官網
值得一提的是,2024 年 8 月 13 日,奧賽康又遞交了利厄替尼的第 2 項適應癥上市申請,用于具有 EGFR 外顯子 19 缺失(19DEL)或外顯子 21 置換突變(L858R)的局部晚期或轉移性 NSCLC 成人患者的一線治療。Insight 數據庫顯示,該申請有望于 2026 年第三季度獲批。
責任編輯/劉秀










評論 0